かんとこうブログ
2020.02.28
新型コロナウイルスの簡易検査方法について、現時点で素人がまとめると
新型コロナウイルスによる感染症で何が不安をあおっているかについては、①検査をなかなかしてもらえない、②感染しても治す薬がない、の2点につきるのではないでしょうか? ②の薬については昨日「アビガン」のことを書きましたので、今日は①の検査について、現在鋭意研究中といわれる簡易検査方法について書きます。最後まで読んでもらうには、少し長くなってしまいました。お許しください。
これまで、コロナウイルスの検出用に検討されている簡易検査方法は2種類と考えられていました。ひとつはLAMP法、もうひとつはイムノクロマト法です。LAMP法は栄研化学が、イムノクロマト法はデンカの子会社デンカ生研が、それぞれ開発着手を発表しています。ところが昨日突如、神奈川県と理研が、新しい時間短縮検査方法の発表を行い、実用化が近いと発表しました。これも併せ3種類の方法について調べたことを書きます。
まず、LAMP法は、栄研化学のサイト内に次の記述がありました。「通常PCR法は DNAを増幅する際に2種類のプライマーを使用し3段階の温度 変化を必要としますが、LAMP法は、4種類のプライマーと鎖置 換活性を持つDNA合成酵素を用い、60~65℃付近の一定温度 でインキュベートするだけで、連続的に反応が進行します。連続 的に反応が進むため増幅効率が高く、短時間(1時間以内)に標 的遺伝子を増幅することができる上、増幅と同時に生成される副 産物による濁りで増幅の様子をモニタリングできることから、増幅・ 検出までの全工程を1チューブ内で終えることができます。」*1)つまり、LAMP法は、PCR法と同じように遺伝子を増幅させて調べるのですが、より簡単な操作で短時間に検出可能にする方法だということです。短時間とは言え15分~1時間はかかるようです。
昨日神奈川県と理研が発表した迅速検出方法である「SmartAmp 法の特長は、従来の PCR 法と比較すると、①等温増幅(PCR のようにサーマ ルサイクルではないため、温度コントロールに大量のエネルギーを必要とせず、機器の小型化に最適)、②高速検出(10-30 分)、 ③増幅の検出で陽性判定できるのでデータ解析がシンプル、④PCR より高い検出特異性、⑤高感度(PCR 法と同等以上)、などの特長を持ちます。」*4)とあり、上で説明したLAMP法とコンセプトは似ており、検査に要する時間の短縮が可能となります。また検出の際の増幅物の可視化にも工夫があるようです。開発そのものは「すでにできた感」がありますが、実証試験、認可といった時期、いつ実用化するのかには言及されていません。
一方イムノクロマト法は、「セルロース膜上を被検体が試薬を溶解しながらゆっくりと流れる性質(毛細管現象)を応用した免疫測定法である。検体中の抗原は検体滴下部にあらかじめ準備された金属コロイド等で標識された抗体(標識抗体)と免疫複合体を形成しながらセルロース膜状を移動し、セルロース膜状上にあらかじめ用意されたキャプチャー抗体上に免疫複合体がトラップされ程色し、それを目視により判定する。妊娠診断、インフルエンザ等で応用されている。」*2) つまり、試験キット上で試験体内の病原(抗原)と免疫(抗原抗体)反応を起こさせ、それを検出するという方法で、簡単な操作とキットで検査できます。具体的な検査操作は以下になります。
「測定法 下図参照 (1)キット上に検体を滴下する (2)一定時間放置する (3)目視による定性判定する(コントロールラインを必ず確認する)」*2)
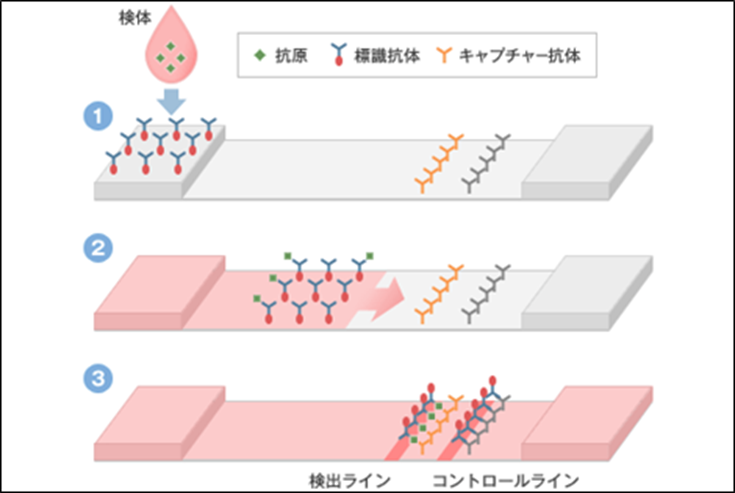
イムノクロマト測定法*2)
こちらの方が簡便かつ短時間になりますが、開発にあたっては、「まず、検体中のウイルス抗原を特異的に認識するモノクローナル抗体を取得し、その上で、作製した抗体を使って、イムノクロマト法の迅速診断キットを製剤化し、キットの臨床性能を調べる臨床評価を実施した上で、承認申請を行う。」*3)であり、それぞれの工程の開発が1年程度要するのではとのことです。時間がかかりそうです。
素人なので、詳しいことはわかりませんが、開発スピードではLAMP法もしくはSmartAmp法、簡便さではイムノクロマト法に優位性があるように思えます。しかし、すぐ明日から使えるというわけにはいかないのであれば、まずは何とかPCR法の処理件数を飛躍的に増大させ、国民の不安を払拭するのが、最も現実的な対処方法ではないかというのが今日の結論です。
こうしたコロナウイルスの検出方法の開発に、何か塗料で培った技術ができるとよいのですが、残念ながらお手伝いの余地はなさそうです。せいぜいイムノクロマト法で検体を展開させるプロセスで何か塗料技術でお手伝いができればといった程度でしょうか?
本項については、「 」内の文章や図を以下のサイトから引用しています。
*1http://www.eiken.co.jp/modern_media/backnumber/pdf/MM0810_01.pdf#search=%27lamp%E6%B3%95+pcr%E6%B3%95+%E9%81%95%E3%81%84%27
*2)https://www.acute-care.jp/ja-jp/learning/course/immunoassay/ria/ic
*3)https://bio.nikkeibp.co.jp/atcl/news/p1/20/02/13/06552/
*4)https://www.pref.kanagawa.jp/documents/59150/200227coronavirus.pdf
「15分で検査ができるキットが販売!」されるのですが・・ 2020年3月13日
昨日の午後2時15分、クラボウ(倉敷紡績株式会社)から「「新型コロナウイルス抗体検査試薬キット」の販売開始について」という発表があり、「コロナウイルスを15分で検査できるキットが販売開始」とネットのニュースが配信されました。直後、同社の株はストップ高となり、同社のホームぺージにはアクセスが集中して接続できない状態となりました。しかしながら、こんな大ニュースが夜のニュースではほとんど報道されることはありませんでした。今日はこの件について書きます。
まず、販売が開始される「検査キット」の概要ですが、本サイトの2月28日付「コロナウイルスに関する簡易検査方法」に関する記事でご紹介した二つの方法のうちのイムノクロマト法を用いた簡易検査キットです。イムノクロマト法というのは、簡単に言えば、試験キット上で病原(抗原)と免疫(抗原抗体)反応を起こさせ、それを検出するという方法です。現在すでにインフルエンザの検査に使用されている方法で、15分程度の短時間で検出可能であり、いわば国民待望の検査キットともいえる簡易検査キットです。
今回発表したクラボウ以外にも日本ではたくさんの研究機関や会社で研究されていましたが、なぜクラボウがいち早く販売開始に漕ぎつけたのでしょうか?そのカギは、このキットが開発された場所にあります。クラボウの発表資料によれば、今回発売するキットは、中国にある提携先企業が開発したもので、これを輸入して販売するとのことです。このキットは、中国における標準診断法の一つとして、すでに中国の診療ガイドラインに採用されているそうです。
なぜ中国なのか?その答えは、抗原であるウイルスの入手の容易さにあると思われます。2月28日の時点では、日本においては、まだコロナウイルスがこうしたキットの開発機関に提供されていないとのことでした。このキットの開発には、ウイルスと免疫を作る抗体の開発が必須であり、このためには研究機関がウイルスを入手できることが必須条件となります。中国では、流行時期が早かったこともあり、ウイルスの入手も日本に比べると格段に早く、それが早期の開発につながったものと思われます。
しかしこのクラボウのキットですが、よく読むと、このキットは「体外診断用医薬品ではなく、ウイルスの抗体の有無をみるための研究用試薬キットとしての使用に限定」されています。つまり、患者の診断には使用できないのです。なぜ使用できないのか? それは、診断や治療に使用されるものは、臨床試験を経て、国の認可を受けなければならないからです。販売先も衛生研究所などの研究・検査機関に限定されており、病院などの医療機関には販売されません。このことが昨晩のニュースで取り上げられなかった理由だと思われます。
現時点では、臨床試験や認可の時期について言及されていませんが、このキットは、PCR法に比べて検体サンプルの採取方法や採取部位の影響を受けにくいという優位性もあり、一刻も早い医療用への認可が待たれるところです。